O insulinoma é o tumor neuroendócrino pancreático funcionante mais frequente (55%), tem seu pico de ocorrência em pacientes na quinta década de vida (entre 40 e 50 anos) e uma discreta predominância entre as mulheres (1,4:1)1.
Os sintomas associados ao tumor se dividem entre adrenérgicos – ansiedade, tremores e agitação – e neuroglicopênicos como desorientação, alterações visuais e convulsões2. Devido a frequente ingestão alimentar para evitar a hipoglicemia acentuada durante o jejum, é frequente que os pacientes se apresentem com obesidade/sobrepeso ao diagnóstico.
Em 1938 foi descrita a tríade de Whipple: hipoglicemia documentada (<50mg/dL), sintomática e aliviada após ingesta calórica. Atualmente, a confirmação diagnóstica se dá com um teste clínico de jejum de 48 a 72 horas em que se coletam exames laboratoriais periodicamente. O perfil laboratorial demonstrará uma glicemia baixa em oposição a elevados níveis de insulina, pro-insulina e peptídeo C3. É fundamental para o diagnóstico se certificar que o paciente não faz uso de antidiabéticos orais como sulfonilureias ou insulina injetável.
A relação do insulinoma em síndromes endócrinas (NEM-1 e esclerose tuberosa) é conhecida e traz particularidades propedêuticas devido a um maior risco de tumores neuroendócrinos múltiplos ou insulinomas malignos4.

O tratamento recomendado é a excisão cirúrgica do tumor. A enucleação, bem como as pancreatectomias segmentares, são tratamentos reconhecidos uma vez que a grande maioria dos tumores são benignos. Dessa forma, a linfadenectomia se torna menos relevante que a preservação de parênquima pancreático a fim de evitar insuficiência exócrina ou endócrina1.
Dessa forma, este artigo pretende trazer uma análise dos diferentes exames diagnósticos utilizados nos casos do insulinoma e suas aplicações, além de uma lista de cuidados perioperatórios específicos para esses pacientes.
Métodos diagnósticos por imagem
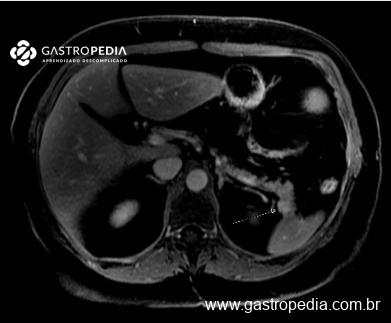
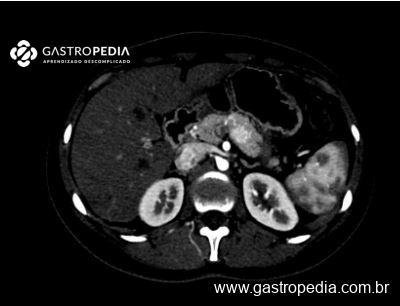
Os métodos axiais com contraste são os mais utilizados para o estudo anatômico do pâncreas e suas relações vasculares. Dentre eles, a ressonância magnética, quando disponível, se provou mais sensível para localizar os insulinomas que se apresentam como nódulos hipervasculares na fase arterial, com hiperintensidade em T2 e hipointensidade em T1 em relação ao parênquima pancreático. Lesões menores podem ser localizadas mais facilmente nas fases de difusão5.
Um exame específico para tumores neuroendócrinos que se vale de seus receptores de somatostatina, o PET Galio 68 pode auxiliar em casos de suspeita clínica sem diagnóstico pelos métodos acima. É um exame adequado para a localização de insulinomas ectópicos que não foram visualizados no abdome superior5.
Métodos diagnósticos invasivos
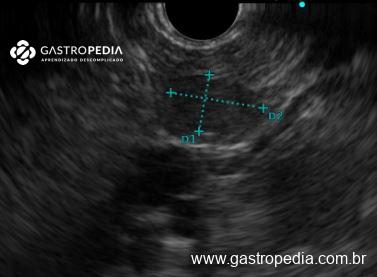
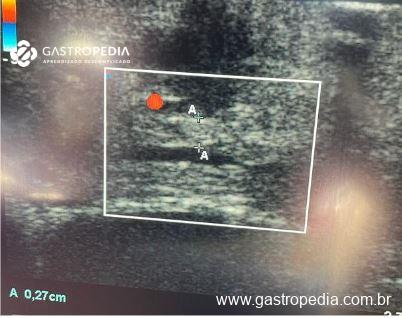
Ecoendoscopia: Exame para avaliação do parênquima pancreático em busca de lesões subcentimétricas, usado por alguns autores como o primeiro exame para se localizar o insulinoma. Oferece sensibilidade ainda maior nas lesões da cabeça do pâncreas e processo uncinado.
No laudo de uma suspeita de insulinoma é importante constar, se possível, a mensuração do tumor, sua localização e a distância de estruturas vasculares relevantes (junção espleno-mesentérica), e da proximidade do ducto pancreático principal (auxiliar a decisão operatória de enuclear a lesão).1
A punção por agulha é dispensável na grande maioria dos casos. O paciente sintomático com lesão esporádica não precisa de confirmação anatomopatológica para o tratamento. Nas síndromes endócrinas, tanto os tumores neuroendócrinos funcionantes quanto os não funcionantes podem expressar marcadores imuno-histoquímicos para insulina. Dessa forma, esse exame não é adequado para diferenciá-los. 6
Em lesões não periféricas ou intrapancreáticas de difícil localização, o cirurgião pode solicitar uma tatuagem com azul de metileno para facilitar a localização intraoperatória.
Cateterismo arterial pancreático seletivo (SACS)
O exame consiste no posicionamento de um cateter coletor na veia hepática direita para coleta do nível sanguíneo de insulina após os estímulos arteriais.
Em seguida, após cateterização arterial seletiva, injeta-se gluconato de cálcio nas artérias peripancreáticas com poder de topografar a lesão caso a insulinemia dobre dentro de 3 minutos após a injeção.
- Tumor na corpo/cauda do pâncreas: Positivo após injeção na artéria esplênica
- Tumor na cabeça pancreática ou processo uncinado: Positivo após injeção na artéria gastroduodenal ou mesentérica superior
- Metástase hepática oculta: Positivo após injeção na artéria hepática própria
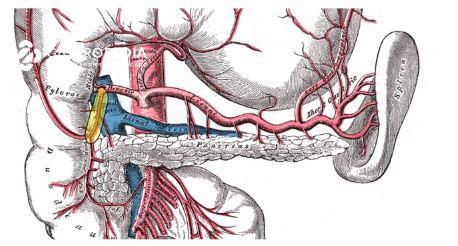
O exame é usado sobretudo em casos de síndromes endócrinas e de tumores neuroendócrinos múltiplos em que se deseja identificar qual a lesão metabolicamente ativa.1
Tratamento operatório
A definição de via operatória depende da expertise do cirurgião. É importante destacar que para o acesso laparoscópico, sobretudo de nodulectomias e pancreatectomias distais, é necessário um planejamento detalhado do local da secção pancreática. A conversão para cirurgia aberta está justificada nos casos de imprecisão.7

A ultrassonografia intra-operatória é uma aliada do cirurgião de fígado e pâncreas e que, nesse contexto, certifica a localização tumoral e a proximidade com ducto pancreáticos nos casos em que se aventa enucleação. Dessa forma, o exame proporciona maior segurança ao procedimento, reduzindo risco de fístula pancreática e permitindo preservação de parênquima pancreático quando possível.
Na cirurgia convencional a inspeção e palpação do órgão pode identificar o tumor que tem uma textura e consistência fibroelástica em um parênquima pancreático mais macio. Para os casos em que se planeja a enucleação, a cápsula do tumor pode ser um parâmetro para o plano de dissecção, e o uso de clipes ou ligaduras é encorajado para que se evite lesão térmica do ducto. 1
Cuidados perioperatórios com a glicemia
Devido ao jejum pré-operatório e a possibilidade de motivar sintomas, encorajamos o uso de soro de manutenção calórica para reduzir eventos de hipoglicemia.
Durante o procedimento, um aumento em 30 mg/dL do platô glicêmico ocorre em até 30 minutos após a ressecção do tumor metabolicamente ativo. A alteração glicêmica somada a análise macroscópica da peça durante o intraoperatório pode confirmar o sucesso do procedimento.
Espera-se um aumento da glicemia nas primeiras 24 horas do procedimento, período em que costumeiramente mantêm-se o soro de manutenção calórica. O monitoramento da glicemia é importante durante a hospitalização e nos primeiros dias após a alta médica. Durante as semanas que sucedem a cirurgia, pode acontecer um aumento da glicemia que demande, inclusive, uso temporário de insulina. 1
Alternativas para tratamento
Em pacientes não candidatos a cirurgia, podemos realizar tratamento clínico com diazoxida (dose inicial de 50 – 300 mg/dia) e análogos da somatostatina (octreotide). Devido a efeitos colaterais dessas medicações, a sua prescrição deve ser feita por profissionais com experiência como endocrinologistas ou oncologistas. As mesmas medicações podem ser utilizadas como tratamento sintomático antes do procedimento ou paliativo no contexto de insulinomas malignos irressecáveis ou metastáticos.2
Tratamento radioablativos endoscópicos ou percutâneos tem emergido como possíveis alternativas em caso de pacientes não candidatos a cirurgia devido a condições clínicas, desde que se preserve uma distância mínima de 3 mm em relação ao ducto principal.
Como citar este artigo
Magalhães, DP. Insulinoma: Estratégias diagnósticas e detalhes para o tratamento. Gastropedia 2022. Disponível em: https://gastropedia.pub/pt/cirurgia/insulinoma-estrategias-diagnosticas-e-detalhes-para-o-tratamento
Quer saber mais sobre TNE do pancreas? Confira esse artigo: Tumores neuroendócrinos do pancreas
Referências
- Mehrabi, A. et al. R EVIEW A Systematic Review of Localization , Surgical Treatment Options , and Outcome of Insulinoma. Pancreas 43, 675–686 (2014).
- Giannis, D. et al. Insulinomas : from diagnosis to treatment . A review of the literature. JBUON 25, 1302–1314 (2020).
- Okabayashi, T. et al. Diagnosis and management of insulinoma. World J. Gastroenterol. 19, 829–837 (2013).
- Habermann, E. B. Malignant Insulinoma : A Rare Form of Neuroendocrine Tumor. World J. Surg. 44, 2288–2294 (2021).
- Prasad, S. R., Kondapaneni, S., Tammisetti, V. S., Nazarullah, A. & Katabathina, V. S. Pancreatic Neuroendocrine Neo- plasms : 2020 Update on Patho- logic and Imaging Findings and Classification. Radiographics 40, 1240–1262 (2020).
- Halfdanarson, T. R. et al. The North American Neuroendocrine Tumor Society Consensus Guidelines for Surveillance and Medical Management of Pancreatic Neuroendocrine Tumors. 49, 863–881 (2020).
- Heidsma, C. M. et al. Indications and outcomes of enucleation versus formal pancreatectomy for pancreatic neuroendocrine tumors. Int. Hepato-Pancreato-Biliary Assoc. 23, 413–421 (2021).
Residência médica em Cirurgia Geral e Cirurgia do Aparelho Digestivo pelo Hospital das Clínicas da FMUSP.
Cirurgião voluntário do Serviço de Pâncreas e Vias Biliares do Hospital das Clínicas - USP.
Cirurgião do Aparelho Digestivo no Hospital Israelita Albert Einstein