Tratamento da Diverticulite Aguda
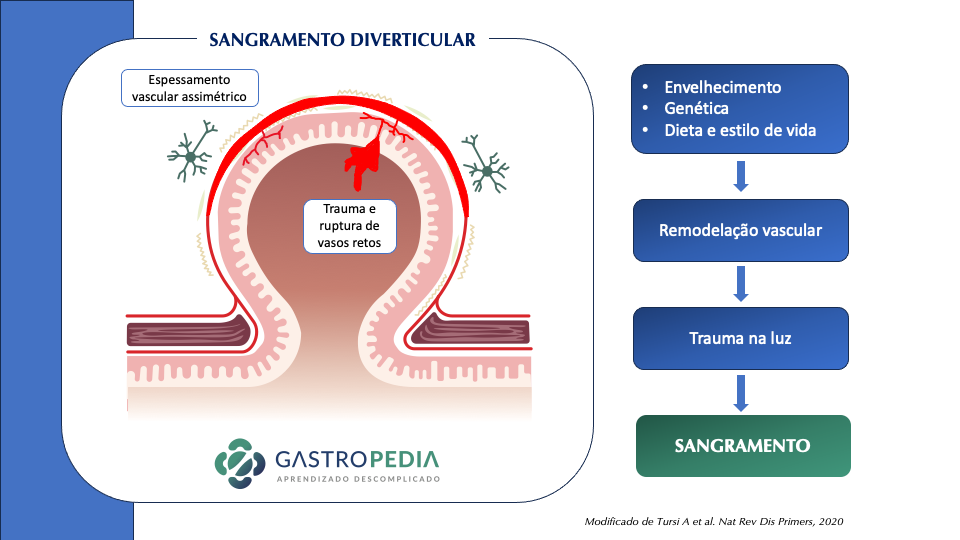
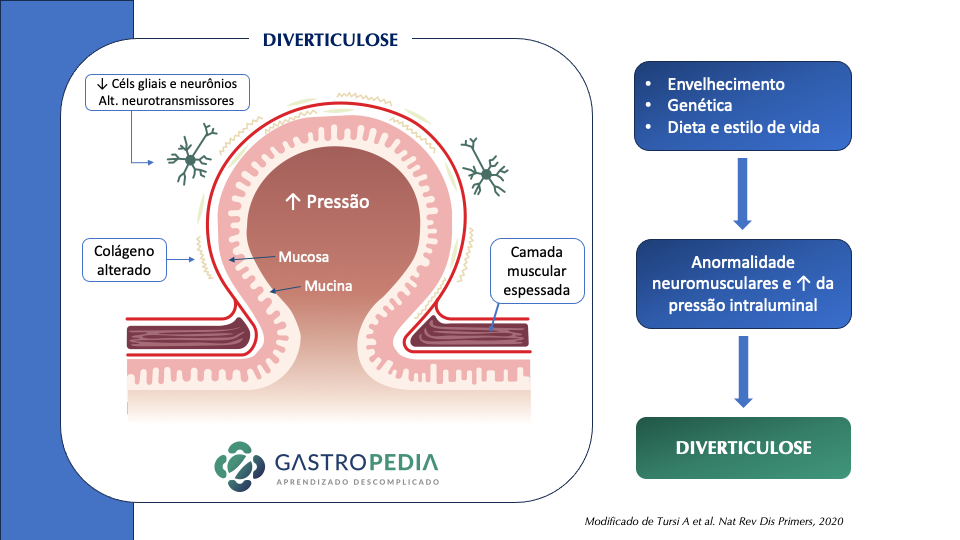
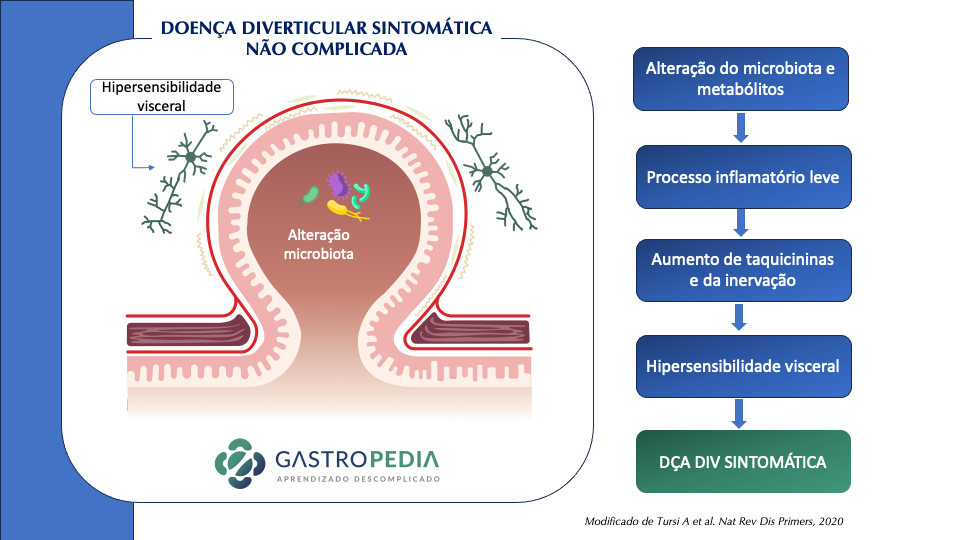
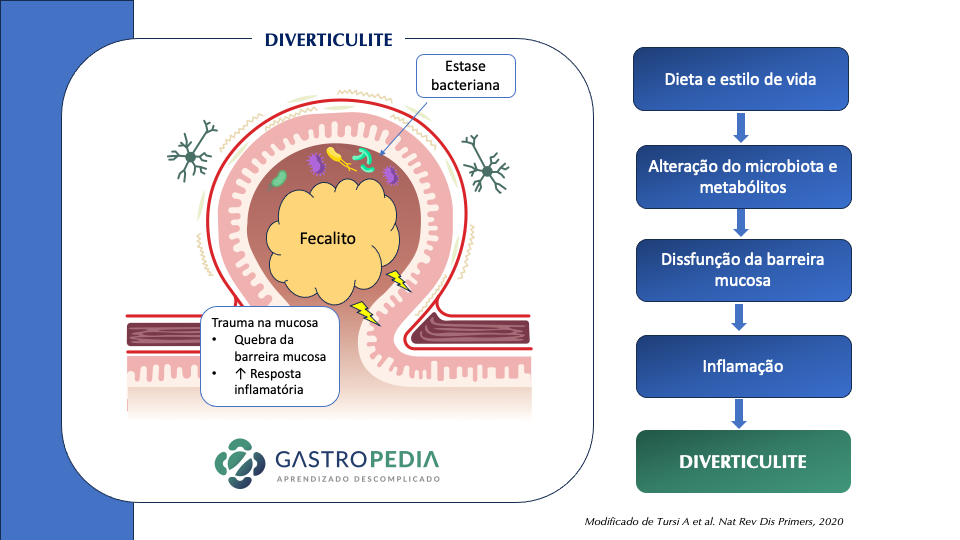
A doença diverticular do cólon é uma causa importante de internações hospitalares e acarreta custos significativos no sistema de saúde das sociedades ocidentais e industrializadas. A fisiopatologia e epidemiologia da diverticulite já foi abordada anteriormente no Gastropedia nesse outro post. Nesse artigo vamos abordar o tratamento da diverticulite aguda.
A primeira decisão acerca do tratamento de um paciente com diverticulite envolve determinar a necessidade de internação ou não.
A diverticulite aguda apresenta-se de forma leve na maioria dos casos. Pacientes com sintomas leves de dor abdominal, sem queda do estado geral, com trânsito intestinal normal e capazes de aceitar dieta oral e com cognição razoável para entender as explicações sobre as indicações de sofrer reavaliação podem ser tratados sem hospitalização. O tratamento ambulatorial é habitualmente eficaz e menos de 10% dos pacientes são readmitidos.
Quadros leves – pacientes não hospitalizados
O tratamento para pacientes não hospitalizados apresenta algumas divergências entre os guidelines e pode incluir dieta líquida (ou leve), hidratação oral e antibióticos (ou não – leia mais sobre o tema clicando aqui ).
Nossa recomendação:
- dieta líquida sem resíduos;
- controle da dor com analgésicos e antiespasmódicos;
- antibióticos de largo espectro por 7-10 dias. Os antibióticos devem cobrir a flora gastrointestinal de gram-negativos e bactérias anaeróbias;
- a maioria dos estudos recomenda como primeira linha a combinação de fluroquinolona (ciprofloxacina 200-400mg/12h) e metronidazol (500mg/8h);
- como alternativa ao metronidazol pode se recorrer à clindamicina (lembrar que estamos falando de ATB vo).
Quando devemos internar?
As seguintes situações reforçam a necessidade de internação hospitalar:
- Diverticulite complicada (perfuração franca, abscesso, obstrução, fístula, etc);
- Sinais de sepse: temperatura >38C, FC > 90, FR > 20, Leucocitose ou leucopenia importante, PCR > 15 md/dL;
- pacientes com maior risco (muito idosos, diabéticos, insuficiência cardíaca, doença renal crônica, doença pulmonar obstrutiva crônica, obesos, com doença do tecido conjuntivo ou imunossuprimidos, aqueles em corticoterapia prolongada);
- pacientes incapazes de tolerar dieta e hidratação oral;
- dor abdominal importante, com suspeita de complicações;
- pacientes sem melhora com tratamento ambulatorial inicial.
Todos os pacientes submetidos a internação devem se submeter a TC e receber ATBterapia.
Tratamento dos pacientes hospitalizados
No tratamento dos pacientes hospitalizados, o jejum (hidratação EV) ou a dieta líquida ou leve são considerados pelos diferentes guidelines a depender do grau da complicação.
Em relação a antibioticoterapia, a via de acesso também é motivo de divergência entre os diversos guidelines, podendo ser utilizado por via oral ou endovenosa. O tempo de uso também varia entre 4 a 10 dias.
Nossa recomendação nos casos não complicados:
- Antibioticoterapia EV (podendo ser alterada para VO quando boa aceitação da dieta no terceiro ao quarto dia), incluindo cobertura para gram positivos, gram negativos, anaeróbios e aeróbios.
- Os esquemas antibióticos mais utilizados são ciprofloxacino (ou Ceftraxione) associado a metronidazol, ou ampicilina + gentamicina + metronidazol.
- Melhora sintomática e laboratorial deve ser esperada em dois a quatro dias quando a dieta pode ser avançada.
- Pacientes sem complicações e que apresentem boa condição clínica podem receber alta e é sugerido completar o uso de antibiótico por pelo menos 7 dias, se estendendo até 14 dias em casos selecionados.
Abordagem do abscesso diverticular (Hinchey I e II)
- A escolha do tratamento depende muito do tamanho do abscesso, da sua localização, se está acessível para drenagem percutânea e a apresentação clínica do doente.
- Abscessos > 3 cm são tratados principalmente com drenagem percutânea, antibioterapia IV, dieta líquida e controle da dor.
- A melhoria significativa na temperatura, dor abdominal e leucocitose geralmente é observada dentro de 48 horas após o início do tratamento.
- A intervenção cirúrgica pode tornar-se necessária se o abscesso não for acessível para drenagem ou se os sintomas persistirem ou piorarem, mesmo com a drenagem. Assim, a cirurgia de urgência com ressecção, continua a ser a única opção bem documentada se o doente estiver instável ou se o tratamento clínico falhar.
- As contraindicações à drenagem percutânea são: peritonite purulenta ou fecal difusa ou coleção sem acesso por abordagem percutânea.
- A drenagem percutânea trata com sucesso 80% dos doentes.
Abordagem de perfuração livre (Hinchey III e IV)
- Os doentes com peritonite generalizada purulenta (Hinchey III) ou peritonite fecal (Hinchey IV) são tipicamente doentes com sintomas e sinais de sepse.
- A fluido terapia agressiva imediata e antibióticos IV de amplo espetro devem ser administrados imediatamente.
- As taxas de mortalidade relatadas são 6% para peritonite purulenta e 35% para peritonite fecal.
- A intervenção cirúrgica de emergência é necessária para controlar a origem da sepse.
Indicação do tratamento cirúrgico de URGÊNCIA na diverticulite aguda
- Falha da terapêutica medicamentosa;
- Diverticulite complicada (perfuração, peritonite);
- Instabilidade ou sepse;
A ressecção com anastomose primária com ou sem ostomia de proteção é hoje considerada o método padrão-ouro pois apresenta vantagens como eliminação foco séptico e absorção sistêmica de toxinas, diminuição da mortalidade operatória geral, redução do número de operações e custo hospitalar, ressecção de segmento que pode albergar câncer e o fato de permitir a lavagem e a drenagem da cavidade de forma mais efetiva, de acordo com o último guideline da Sociedade Americana de Cirurgiões Colorretais (ASCRS) (Hall J, et al. Dis Colon Rectum. 2020). Entretanto, a escolha da técnica cirúrgica depende da estabilidade hemodinâmica do paciente, da extensão da contaminação peritoneal e da experiência do cirurgião. Muitos serviços ainda recomendam a cirurgia de Hartmann em casos de peritonite fecal.
Aspectos técnicos da cirurgia
Em relação aos aspectos técnicos da cirurgia, existe uma concordância entre todos os guidelines que a margem proximal da ressecção deve ser em tecido saudável, não havendo a necessidade de retirar todo cólon remanescente apenas porque existem divertículos no mesmo.
Já a margem distal deve ser em reto proximal, abaixo da transição retossigmoide.
A anastomose colorretal deve ser realizada em tecido são, e não deve incluir divertículos na linha de grampeamento (ou de sutura).
A artéria mesentérica inferior deve ser preservada quando não há suspeita de malignidade.
Não há consenso em relação a mobilização da flexura esplênica. Entretanto, na disciplina de Coloprocotolgia do HCFMUSP preconizamos a mobilização de rotina da flexura esplênica para confeccionar a anastomose sem tensão.
É essencial a identificação dos ureteres e dos nervos pré-sacrais, assim como a manutenção da vascularização apropriada, evitando-se a dissecção do mesentério friável.
Dificuldade cirúrgicas na diverticulite aguda:
- Presença de abscessos, coleções e aderências secundárias ao processo inflamatório e infeccioso
- Distorções anatômicas
- Trajetos fistulosos podem estar presentes
- Friabilidade dos tecidos
- Os pacientes tendem a ser idosos e com comorbidades associadas
- Muito dos pacientes são obesos com bastante gordura visceral

Conheça nosso curso Gastroenterologia do Consultório e saiba como lidar com as queixas mais comuns que encontramos no dia a dia
Referências
- Hall J, Hardiman K, Lee S, Lightner A, Stocchi L, Paquette IM, Steele SR, Feingold DL; Prepared on behalf of the Clinical Practice Guidelines Committee of the American Society of Colon and Rectal Surgeons. The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for the Treatment of Left-Sided Colonic Diverticulitis. Dis Colon Rectum. 2020 Jun;63(6):728-747.
- Tursi A, Scarpignato C, Strate LL, Lanas A, Kruis W, Lahat A, Danese S. Colonic diverticular disease. Nat Rev Dis Primers. 2020 Mar 26;6(1):20. doi: 10.1038/s41572-020-0153-5. PMID: 32218442
Como citar este artigo
Martins BC e Camargo MGM. Tratamento da Diverticulite Aguda Gastropedia 2023; vol 2. Disponível em: gastropedia.pub/pt/cirurgia/tratamento-da-diverticulite-aguda/