Quando devo me preocupar frente a um cisto hepático?
Introdução
Cistos hepáticos são achados comum em exames de imagem, e muitas vezes podem ser motivo de ansiedade e preocupação ao paciente. Muito embora os cistos hepáticos simples – de caráter completamente benigno – sejam as lesões hepáticas mais frequentes, acometendo 20% da população em geral, até 5% dos cistos podem corresponder a cistadenomas ou cisto-adenocarcinomas biliares, lesões que são associadas a malignidade. Neste artigo vamos entender mais sobre estes cistos malignos do fígado, quando suspeitá-los e como tratá-los.
Cistadenomas biliares ou cisto-adenocarcinomas biliares são lesões císticas raras que acometem o parênquima hepático, ou, menos comumente, a via biliar extra hepática e que apresentam, em seu interior, presença de estroma ovariano. Também podem ser chamados de neoplasia cística mucinosa do fígado (NCMF) ou neoplasia cística mucinosa associada a carcinoma invasivo.
Quadro Clínico
Desde que os critérios diagnósticos de NCMF foram revisados em 2010 com relação à presença de estroma ovariano, vários estudos têm reportado apresentação quase que exclusiva em mulheres.
A maioria dos pacientes é assintomática. Entretanto, há uma pequena parcela que pode apresentar sintomas provocados pelo efeito de massa do cisto quando atinge grandes dimensões e comprime órgãos adjacentes. A compressão do estômago/duodeno pode levar a empachamento/saciedade precoce, e até a quadros de náuseas e vômitos pós alimentares. A compressão do gradil costal pode provocar dor. E a compressão da via biliar principal pode gerar quadros colestáticos.
Laboratorialmente, a maioria dos pacientes apresenta resultados normais; entretanto, há uma pequena porcentagem que pode apresentar bilirrubinas e enzimas hepáticas e/ou canaliculares alteradas.
Diagnóstico Diferencial
O diagnóstico diferencial é amplo, e inclui cistos hemorrágicos, cistos hidáticos, IPMN-biliares, abscessos hepáticos, doença policística, tumores malignos degenerados, tumores metastáticos produtores de mucina, hemangiomas císticos, linfangiomas, e um cisto simples atípico.
O IPMN-biliar pode ser diferenciado da NCMF baseado em fatores de imagem, tais como:
| Neoplasia Cística Mucinosa do Fígado (NCMF) | Neoplasia Intraductal Papilífera da via biliar (IPMN-B) | |
|---|---|---|
| Achados de Imagem | Massa cística multilocular, com aparência de cistos menores dentro da parede do cisto. | Muticístico, com aparência semelhante a cacho de uva, com nódulos papilares e dilatação biliar periférica. |
| Comunicação Ductal | Geralmente ausente | Presente |
| Estroma | Ovariano | Fibroso |
| Potencial Maligno | Baixo | Alto |
Estudos de Imagem
Tendo em vista o amplo diagnóstico diferencial, os exames de imagem têm um papel fundamental na avaliação destes pacientes.
Vale ressaltar que são características importantes da NCMF: cisto solitário, septado, localizado no lobo esquerdo, preferencialmente no segmento IVb.
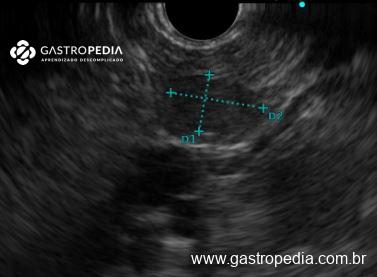
Frequentemente usado como método inicial, o ultrassom (US) tem uma sensibilidade de 90% para a caracterização de uma NCMF. Especificamente no US, a NCMF se manifesta como uma massa cística de grandes dimensões (tamanho médio de 11cm), multilocular, com paredes assimetricamente espessas e com septos ecogênicos. Pode haver nódulos murais na parede dos cistos. A presença de nódulos murais, debris intracísticos e dilatações de ductos biliares favorece a presença de transformação maligna.
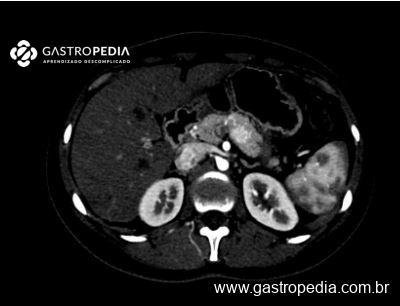
Na tomografia, a NCMF aparece como uma massa cística grande, bem delimitada, multiloculada, com uma cápsula fibrótica claramente definida. Calcificações murais e irregularidades ou nódulos murais que captam contraste são característicos. Dilatação biliar e cistos solitários são características da NCMF. De 69% – 76% dos casos ocorrem no lado esquerdo do fígado, com uma clara preferência pelo segmento IV. Um exemplo dos achados de imagem típicos está na Figura 1.
Um estudo demonstrou capacidade de diferenciação entre cistos biliares simples e NCMF, com sensibilidade e especificidade de 87%, usando 2 dos 5 seguintes critérios:
- Presença de septos
- Septos centrais
- Nódulos murais
- Dilatação biliar proximal
- Dilatação biliar distal

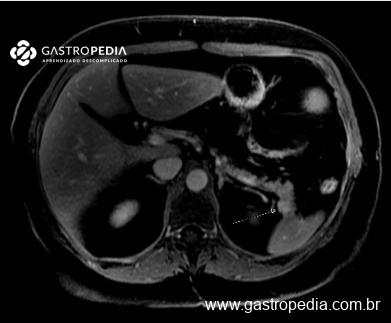
A ressonância magnética (RM) é muito útil na avaliação dessas lesões. Em geral, a NCMF aparece multilocular, com paredes espessas e irregulares. A RM é melhor que a TC para demonstrar realce capsular, septal ou nodular. Uma característica muito sensível da NCMF é a presença de realce ao contraste nos septos. A presença de malignidade já instalada pode ser indicada pela presença de nódulos ou componente sólido maior que 1cm. A colangiopancreatografia por ressonância magnética é útil para estudar a presença ou não de comunicação da lesão com a via biliar (e portanto no diferencial com IPMN-B) e para se obter um mapa de toda a via biliar, estudando se há ou não dilatação do segmento biliar que tenha relação com o cisto.
Marcadores Tumorais
A aspiração de conteúdo do cisto para análise laboratorial é uma forma importante de se auxiliar no diagnóstico. Há estudos que apontam que o CA 19-9 e CEA podem estar elevados no líquido do cisto. Outros dão mais importância à dosagem do CA 72-4 no líquido do cisto.
Tratamento
O cistadenoma biliar é uma lesão pré-maligna que não pode ser diferenciada com segurança do cisto-adenocarcinoma biliar apenas por métodos de imagem ou não invasivos; desta forma, o tratamento para as duas condições é o mesmo: ressecção cirúrgica com margens livres. Métodos não excisionais, como destelhamento, fenestração, esclerose com injeção de substâncias e etc são pouco eficazes, com uma taxa de recidiva que pode chegar a 90%.
A ressecção cirúrgica com margens livres pode ser obtida através de hepatectomias regradas ou através de enucleações ou ressecções não regradas. A escolha vai depender da posição da lesão cística e de sua relação com estruturas vásculo-biliares intra-hepáticas.
A literatura reporta taxa de recorrência de 1% a 5% para lesões ressecadas cirurgicamente. A taxa de recidiva após destelhamento deste tipo de cisto pode chegar a 100%.
Se comparado a outros tumores malignos primários do fígado, tais como hepatocarcinoma e colangiocarcinoma, a ressecção cirúrgica das NCMF oferece um prognóstico muito melhor. Muito embora a ressecção de cistoadenocarcinomas biliares tenha um prognóstico pior que a de cistadenomas biliares, o prognóstico ainda é muito melhor que para a ressecção de hepatocarcinoma ou de colangiocarcinoma.
Não há recomendações baseadas em revidência a respeito do uso de tratamento sistêmico ou adjuvante para pacientes com este tipo de tumor.
Conclusão
É importante lembrar que nem todos os cistos hepáticos são completamente benignos. O diagnóstico de neoplasia cística mucinosa do fígado deve ser sempre tido como diferencial possível, especialmente para pacientes do sexo feminino que se apresentam com lesões císticas, multisseptadas, com paredes espessas e localizadas no lobo esquerdo do fígado, mais especificamente no segmento IV. Nesse cenário, a hipótese diagnóstica de neoplasia cística mucinosa do fígado deve ser considerada, e o tratamento cirúrgico excisional deve ser proposto à paciente.
Referências
- Aziz H, Hamad A, Afyouni S, Kamel IR, Pawlik TM. Management of Mucinous Cystic Neoplasms of the Liver. J Gastrointest Surg. 2023 Sep;27(9):1963-1970. doi: 10.1007/s11605-023-05709-6. Epub 2023 May 23. PMID: 37221388.
- Hutchens JA, Lopez KJ, Ceppa EP. Mucinous Cystic Neoplasms of the Liver: Epidemiology, Diagnosis, and Management. Hepat Med. 2023 Mar 29;15:33-41. doi: 10.2147/HMER.S284842. PMID: 37016682; PMCID: PMC10066895.
Como citar este artigo
de Meira Junior, JD. Quando devo me preocupar frente a um cisto hepático? Gastropedia; 2025 Vol 1. Disponível em: https://gastropedia.pub/pt/cirurgia/hepatopancreatobiliar/quando-devo-me-preocupar-frente-a-um-cisto-hepatico